體外診斷產品相關原材料(一) -1
1引言
體外診斷產品的質量很大程度上是由上游的核心原材料決定的。
廣義的原材料包括儀器上游的核心元部件和試劑上游的生物活性/非生物活性材料。狹義的診斷試劑原料一般僅指生化、免疫或分子診斷試劑的反應體系原料,包括核心反應體系、信號體系、載體,以及反應環境等。其中,核心反應體系原料如診斷酶、引物、抗原、抗體等,是體外診斷試劑產業上游最重要的戰略節點,其質量是決定體外診斷試劑質量的最重要因素。信號體系如膠體金、酶底物系統、發光物質等是將不可見的生物反應過程和結果變成可視、可讀的結果的實現環節。反應體系載體如NC膜、酶標板、磁珠等提供了生物化學反應發生的場所,并因各種材料的迥異性能,使得診斷試劑具有快速、高通量、均相等豐富特性。反應環境是由各種生物活性材料和精細化學原料,包括牛血清白蛋白、阻斷劑、氯化鈉、碳酸鈉和各種氨基酸以及有機酸等調配而成的體外診斷試劑緩沖溶液,為試劑的反應排除干擾、為儲存提供了穩定性,保障反應得以順利進行。
本章重點討論核心反應體系原料、信號體系、載體,以及阻斷劑等。有機無機化學原料對診斷試劑品質也有不可忽略的影響,但因原料本身的質量控制和判斷相對簡單,本章不展開。
2診斷試劑原料的國際發展狀況
原料的重要性使得有能力為體外診斷工業提供創新、優質、穩定、大批量的原料的公司異軍突起,越來越受到體外診斷試劑廠商的重視和青睞。不同于科研試劑供應商動輒數十萬產品的“大而全”,體外診斷試劑原料供應商往往“小而美”,這是行業特點決定的。首先,“原料”概念跨度較大,抗原抗體、酶底物、膜材微粒等,涉及完全不同的領域,原料供應商窮究幾十年也往往只精通其中一個領域,比如HyTest主攻單抗,MBC和IIC專做多抗,Genzyme以酶為業,Millipore因膜聞名……。其次,目前被批準使用于臨床檢驗的項目不過千余種(《醫療機構臨床檢驗項目目錄2013版》收錄檢驗項目約1500個),從原料角度進行方法學歸類,則無非化學反應、酶底物反應、抗原抗體反應、PCR反應等數種原理,因而,原料公司的產品數量都相對有限,以國內產品種類數量最多、涉足領域最廣的體外診斷核心原料供應商菲鵬為例,2016年財報顯示經數十年的技術革新和發展,目前已擁有700余小類的抗原抗體產品——比起科研抗體供應商,這十數年積累的產品數量可說是精選嚴選的產物。再次,體外診斷涉及的疾病范圍廣泛,傳染病、腫瘤、心血管、代謝等每一類疾病都代表獨立的學科,作為抗原抗體原料供應商,只有對該疾病和疾病標志物進行長期、專注的研究,才能研發優質的原料應用于疾病診斷,這進一步使得免疫原料的源頭供應商通常僅專精于少數幾個疾病領域,如HyTest擁有毋庸置疑的心血管原料第一品牌定位,BioVentix以Vit D聞達于業界,而Microbix則憑ToRCH抗原獨樹一幟。
當然,隨著頻繁的并購活動,原料供應商中也不乏“巨無霸”的身影,如Merck,BBI,ThermoFisher,Meridian等,產品線橫跨多個領域,為體外診斷工業提供更為完善的解決方案;還有一些公司,如Fitzgerald,Abcam等,擁有超長產品線,他們既服務于工業客戶,也服務于科研客戶。
2009-2016年國內體外診斷市場規模的復合增速為16.60%,預計2016年達到370億元。如果按照診斷試劑原料市場規模約占體外診斷試劑市場規模10%左右計算,我國診斷試劑原料市場規模約37億元。
高速增長的中國體外診斷市場受到國際原料廠商的高度重視,Merck、Roche、東洋紡、HyTest等較早在國內設立子公司,專為中國市場服務;2016年新進入或正在設立中國子公司的有Medix、Meridian、BBI等。其他未進入中國的原料企業,其產品在國內也均可通過代理商如佰橋瑞景和雅為世紀較方便地獲得。而國內的明星原料企業如菲鵬生物,2016年在新三板上市,年銷售額超過1.5億元人民幣,已然躋身國際品牌行列,共同為中國體外診斷試劑工業服務。
可以這么說,中國體外診斷工業,在核心原料這一環節,正與世界同步。
3診斷試劑原料
1 核心反應體系(抗原、抗體、酶)
1. 抗原抗體
抗原抗體廣泛應用于以免疫反應為基本原理的診斷試劑中。抗原抗體反應具有可逆性、最適比例、特異性和敏感性等特點。
(1)可逆性:抗原與抗體結合形成抗原抗體復合物的過程是一種動態平衡,抗原抗體復合物的解離程度與抗體的親和力K值有關。高親和力抗體的抗原結合點與抗原的決定簇在空間構型上非常適合,兩者結合牢固,不易解離。
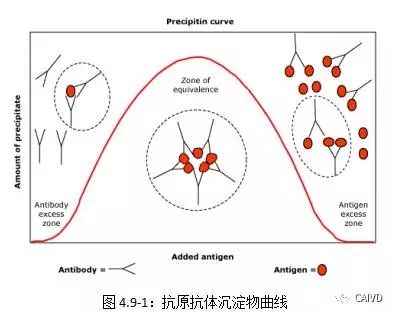
(2)最適比例:在恒定量的抗體中加入遞增量的抗原形成免疫復合物(沉淀)的量見圖4.9-1。曲線的高峰部分是抗原抗體比例最合適的范圍,稱為等價帶(zone of equivalence)。在等價帶前后分別為抗體過剩帶和抗原過剩帶。如果抗原或抗體極度過剩,則無沉淀物形成,在免疫測定中稱為帶現象(zone phenomenon)。抗體過量稱為前帶(prezone),抗原過量稱為后帶(postzone)。在用免疫學方法測定抗原時,應使反應系統中有足夠的抗體量,否則測得的量會小于實際含量,甚至出現假陰性。
(3)特異性:抗原抗體的結合實質上只發生在抗原的抗原決定簇與抗體的抗原結合位點之間。由于兩者在化學結構和空間構型上呈互補關系,所以抗原抗體反應具有高度的特異性。例如乙肝病毒中的表面抗原(HBsAg)、e抗原(HBeAg)和核心抗體(HBcAg),雖來源于同一病毒,但僅與其相應的抗體結合,而不與另外兩種抗體反應。抗原抗體反應的這種特異性使免疫測定能在非常復雜的蛋白質化合物(例如血清)中測定某一特定的物質,而不需先分離待檢物。
但是這種特異性也不是絕對的。假使兩種化合物有著部分相同的結構,在抗原抗體反應中可出現交叉反應。例如:絨毛膜促性腺激素(hCG)和黃體生成激素(LH)均由α和β兩個亞單位組成,其結構的不同處在β亞單位,而兩者的α亞單位是同類的。用hCG免疫動物所得的抗血清中含有抗α-hCG和抗β-hCG兩種抗體,抗α-hCG抗體將與LH中的α酶位發生交叉反應。在臨床檢驗中,如用抗hCG抗血清作為妊娠診斷試劑檢定尿液中hCG,只能用于hCG濃度較高的試驗,否則婦女生理性排泄入尿液中的微量LH將與之發生交叉反應。因此在作為早孕診斷的試劑中必須應用只對hCG特異的抗β-hCG,以避免與其它激素的交叉反應的發生。
(4)敏感性:在測定血清中某一物質的含量時,化學比色法的敏感度為mg/ml水平,酶反應測定法的敏感度約為5~10μg/ml,免疫測定中凝膠擴散法和濁度法的敏感度與酶反應法相仿。標記的免疫測定的敏感度可提高數千倍,達ng/ml甚至pg/ml水平。
因此,抗原抗體反應中原料的靈敏度、特異性、效價和親和力是決定試劑盒性能的關鍵因素,也是試劑生產商對原料性能考核的重點參數。
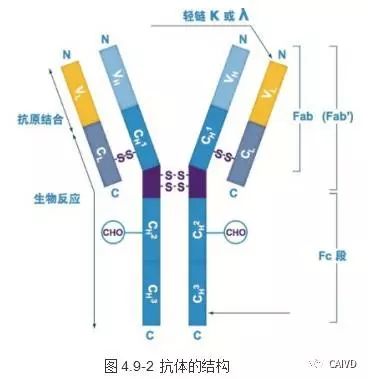
抗體,也叫免疫球蛋白(immunoglobulin),是一種能特異性結合抗原的糖蛋白,而抗原則是在易感染動物體內引發抗體產生的物質。抗體的結構如圖4.9-2所示,一個抗體分子上的兩個抗原結合部位是相同的,位于兩臂末端稱抗原結合片段(antigen-binding fragment,Fab)。“Y”的柄部稱結晶片段(crystalline fragment,FC),糖結合在FC上。另外,FC片段具有抗原性,可被其他抗體或抗體片段所識別。
根據“Y”形結構的數量和重鏈種類的不同,哺乳動物體內的抗體可以分為5類:IgG、IgM、IgA、IgD、IgE。其中IgM是5聚體,而IgA有二聚體三聚體等多種形式。各類抗體在生物學特性、功能區域以及結合不同抗原的能力上有所不同,這里不再贅述。值得一提的是目前在免疫學檢測試劑開發中,主要使用的抗體為IgG,IgM次之。
關于抗體的應用,早在幾百年前便有記載。公元16世紀我國已有關于種痘預防天花的記載;18世紀后葉,英國人Jenner也通過接種牛痘預防天花。而隨著疫苗的應用,抗體的靶向作用也被應用到了更多領域。1890年,白喉毒素的發現,開創了抗體制藥領域;1975年,來源于小鼠B淋巴雜交瘤細胞的第一代單克隆抗體誕生,使得抗體作為疾病診斷和治療的應用范圍有了更大范圍的擴展。
隨著抗體在疾病診斷方面的應用發展,目前主要應用的抗體以鼠、羊和兔子等動物來源的單克隆抗體和多克隆抗體為主。關于單抗和多抗,其定義如下:抗原上可以引起機體產生抗體的分子結構叫做抗原決定簇,也稱為抗原表位。一個抗原可以有許多不同的抗原決定簇,因此,機體也可以產生多種不同的抗體。由單一B淋巴細胞克隆產生的高度均一、僅識別某一特定抗原表位的抗體,稱為單克隆抗體。而由多個B淋巴細胞克隆產生的、受到多種抗原決定簇刺激并可以與多種抗原表位結合的抗體就是多克隆抗體。從某種角度而言,多抗是多種單抗的混合物。
除了定義不同之外,兩者在制備上也有區別。經過特定抗原處理過的B淋巴細胞與骨髓瘤細胞通過細胞融合的方法得到雜交瘤細胞,經HAT培養基篩選、ELISA檢測效價后就可得到陽性克隆株,最后進行細胞培養或將細胞注入到動物(一般為balb/c小鼠)腹腔中用腹水培養,收集上清/腹水純化后就能得到單克隆抗體。而制備多克隆抗體工藝相比于單克隆抗體則簡單許多,只需將抗原(純度越高越好)直接注入到動物體內進行免疫,經過3~4次免疫,ELISA測其效價合格后,收集血液離心得到上清,純化后即能得到多克隆抗體。因此制備多克隆抗體的周期相比單克隆抗體要短,而且首次制備價格也比單抗要低。
在應用方面,單抗和多抗都有各自鮮明的特點與優勢。單克隆抗體的特異性高,一旦制備成功就可以永續的生產完全一致的抗體,因此可以對其特異性進行全面、系統地驗證。但如果所識別的抗原表位被破壞,實驗的結果將會受到很大的影響,這也是單抗的缺點之一。而多克隆抗體的特異性較差,即使是使用相同的抗原制備多抗,不同批次間也會存在差異,因而在特異性、一致性方面有很大的局限。所以在用多抗做免疫檢測時,更容易造成本底過高的現象。雖然多抗存在交叉反應的問題,但由于多抗識別多個抗原表位,即使是有少數幾個抗原表位被破壞或者抗原構象改變,實驗的結果也不會受到影響。因此在相同條件下,使用多抗可以提高檢測的靈敏度,對于豐度偏低的蛋白也更容易檢出。
-
儀器推薦

-
儀器推薦

-
儀器推薦

-
儀器推薦

-
儀器推薦

-
焦點事件