“聲光閃爍療法”治療人類阿爾茨海默癥
阿爾茨海默癥(AD)是一種發病隱匿的進行性神經系統退行性疾病,俗稱老年癡呆癥。根據國際阿爾茨海默癥協會的數據顯示,每3秒鐘,全球就有一位AD患者產生。我國每年至少有30萬新發病例,目前患者數已超過1000萬,占世界AD患者總人口的1/4,而這一數字還在隨人口老齡化攀升。
令人遺憾的是,這一領域至今仍未能揭開阿爾茲海默癥發病的具體機制,更不用說開發有效的治療方法或藥物了。
然而,科學家們從未放棄過努力。
近日,發表在阿爾茲海默癥協會旗下期刊《阿爾茨海默癥與癡呆癥:轉化研究與臨床干預》上的一項研究中,來自美國佐治亞理工學院生物醫學工程系助理教授Annabelle Singer領導的研究團隊開展了首個關于“聲光閃爍療法”治療人類阿爾茨海默癥的臨床試驗,并取得一些引人注目的結果。

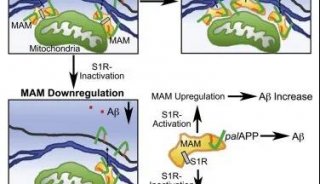
在過去幾年里,Singer的團隊一直致力于用閃爍的光和聲音來治療阿爾茨海默癥(AD)小鼠模型。他們發現,伽馬波(特別是40赫茲)的閃爍光線和聲音能驅動多個大腦區域的伽馬頻率神經活動,并減少AD小鼠模型中的淀粉樣蛋白病理學。這些變化與小膠質細胞(大腦的主要免疫細胞)的轉變、免疫激活和認知功能改善有關。這些研究提出了一種潛在治療AD的新方法,但伽馬波閃爍對人類AD病理和免疫系統的影響尚不清楚。
不同頻率的腦電波似乎與特定的神經功能有關。伽馬波(γ波)以每秒30到100赫茲的頻率振蕩,通常在我們集中注意力或編碼和檢索記憶時可以被觀察到,它與高級認知功能有關。不僅是阿爾茲海默癥,在各種神經系統疾病中都存在伽瑪波紊亂的現象。

先前的研究表明,當人類大腦感覺區域受到幾秒鐘到幾小時的刺激時,連接會加強。然而,對于阿爾茲海默癥治療可能需要的長時間的伽瑪感覺刺激,這意味著人類受試者能否在更長的持續時間內可靠地進行這種刺激是一個關鍵問題。
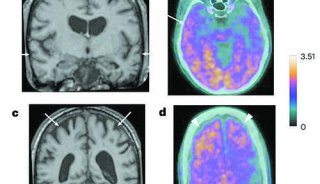
為此,該團隊與埃默里大學的研究人員合作,在埃默里大學腦健康中心開展了一項小規模可行性研究。他們招募了10名輕度認知障礙的AD患者,隨機分為兩組,8周組患者在8周內每天1小時接受40赫茲的“聲光閃爍治療”(佩戴實驗用眼鏡和耳機),4周組的實驗延遲4周開始,持續4周。所有參與者在基線時接受了靜脈抽血、腰椎穿刺(檢查腦脊液)、磁共振成像 (MRI) 掃描、腦電圖 (EEG) 和認知測試。研究人員測試延長伽瑪閃爍刺激的安全性、耐受性,以及輕度認知障礙患者在家使用期間的依從性和確認的AD生物標志物,包括β淀粉樣蛋白、總tau蛋白和磷酸化tau蛋白。

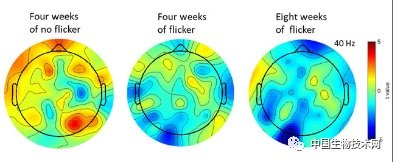
試驗結果表明,“聲光閃爍療法”安全且耐受性良好。患者們均完成了完整的治療計劃。正如研究人員所預期的那樣,在每次研究隨訪期間,所有參與者均由40赫茲的“聲光閃爍”誘導出現了廣泛的腦波夾帶,腦波夾帶被認為是大腦活動與外部刺激同步,會導致大腦產生被稱為雙耳搏動的特殊脈沖,可以改變腦波模式,引起情緒和思維等改變。平均而言,64個通道中有49個產生了腦波夾帶效應。
患者的依從性也很好,依從率達到了約90%左右,在研究期間和后續擴展研究的10個月中沒有嚴重不良反應的報告。一些患者甚至自愿在研究結束后繼續接受監測和評估。
一些患者報告說,治療可能會引起輕微的不適,如頭暈、耳鳴和頭痛。但總體而言,該設備的安全性非常好。
研究人員研究了默認模式下的大腦網絡連接,即在清醒靜息和記憶期間特別活躍的不同大腦區域如何相互作用。AD患者的神經網絡存在缺陷,但經過8周的治療,默認模式下的網絡連接得到加強。
Singer說:“這可能表明這些區域之間有了更強的相互作用,因此通信更好。”
與小鼠研究一樣,聲光閃爍療法也在人體中得到了免疫應答,它激發了細胞因子(用于細胞信號傳導的蛋白質)的活性。這表明該療法已經激活了大腦的免疫系統。
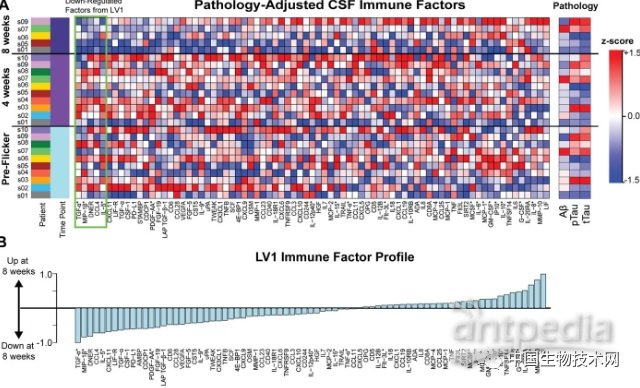
Singer 說:“這是我們想要看到的,因為小膠質細胞可以清除病原體。有些研究認為阿爾茨海默癥的部分原因是這種清除機制失效”。
Singer團隊下一步將了解更長時間的人體試驗是否會產生其他影響,例如淀粉樣蛋白活性是否會降低。
他們表示,到目前為止,這項研究還是非常初步性的,距離得出該療法的臨床益處結論還有一段距離。但這項初步結果帶來了希望,并為更大規模和更長時間的研究奠定了好的基礎。