Nature Medicine:淋巴結靶向的癌癥疫苗,延緩胰腺癌和結直腸癌復發
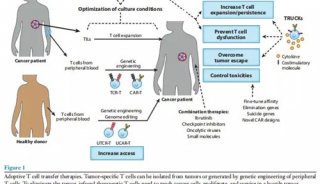
近年來,癌癥免疫療法蓬勃發展并取得了一系列重大突破,許多新型免疫療法被不斷開發完善,例如CAR-T療法、癌癥疫苗,為廣大癌癥患者帶來新的希望。?
在眾多癌癥類型中,結直腸癌和胰腺癌分別是癌癥死亡的第二大和第三大原因,患者的五年生存率低于20%,這些患者在接受過手術治療并完成化療后,仍有很高的腫瘤復發風險,并且一旦復發更難治愈。因此,開發一種預防結直腸癌和胰腺癌復發的腫瘤免疫療法無疑是十分迫切進且重要的。?
近日,美國德克薩斯大學MD安德森癌癥中心、紀念斯隆-凱特琳癌癥中心及Elicio Therapeutics的研究人員聯合多家研究機構,在?Nature Medicine?期刊發表了題為:Lymph-node-targeted, mKRAS-specific amphiphile vaccine in pancreatic and colorectal cancer: the phase 1 AMPLIFY-201 trial?的研究論文。?
這項研究開展了一項1期臨床試驗,所測試的一款癌癥疫苗ELI-002 2P,表現出可預防KRAS突變的結直腸癌和胰腺癌復發的潛力。ELI-002 2P是一種淋巴結靶向的癌癥疫苗,旨在通過“訓練”T細胞識別KRAS突變,使它們能夠識別和清除KRAS突變的癌細胞,從而降低腫瘤復發的可能性。?

KRAS是癌癥中最常見的突變基因之一,該基因突變存在于四分之一的實體腫瘤中,并且在肺癌、結直腸癌和胰腺癌(90%為KRAS突變)等致命性癌癥中突變率更高。因此,KRAS驅動突變(mKRAS)是這一類腫瘤生存所需的、有吸引力的免疫治療靶點。?
已有研究開發出mKRAS導向的過繼T細胞療法,并在癌癥患者中成功誘導了免疫應答。然而,T細胞療法僅限于特定突變和人類白細胞抗原(HLA)等位基因,制備工藝復雜且成本高昂,并伴有潛在的細胞因子釋放綜合征和神經毒性。相比之下,癌癥疫苗接種提供了在不同HLA背景下擴大內源性mKRAS導向T細胞的潛力,并且制造簡單,可用性高。?
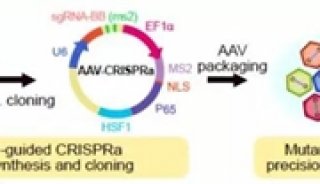
在這項研究中,研究團隊開發了一款針對結直腸癌和胰腺癌的、淋巴結靶向的mKRAS特異性癌癥疫苗——ELI-002 2P。該疫苗通過兩親性(Amph)修飾的KRASG12D和KRASG12R突變肽(Amph-peptides-2P)和CpG寡核苷酸佐劑(Amph-CpG-7909)增強淋巴結遞送和免疫應答。?

癌癥疫苗ELI-002 2P的生產過程和作用機制?
研究團隊圍繞ELI-002 2P開展了一項1期臨床試驗,主要終點包括安全性和推薦的2期劑量,次要終點是腫瘤生物標志物反應(縱向ctDNA或血清腫瘤抗原),探索性終點包括免疫原性和無復發生存期(RFS)。?
在這項1期臨床試驗中,共有25名癌癥患者(20例胰腺癌,5例結直腸癌),中位年齡為61歲,84%是白人,8%是亞洲人,還有2名患者(8%)種族不詳,60%患者為女性。這些患者此前都接受過手術治療,其中7人接受過放射治療,但他們在治療后的最小殘留mKRAS檢測(ctDNA和血清腫瘤抗原)呈陽性。?

1期臨床試驗的參與者?
這些具有高復發風險的癌癥患者接受了最多10劑ELI-002 2P疫苗,其中21例(84%)出現T細胞應答,6例觀察到腫瘤生物標志物減少,中位數無復發生存期(RFS)為16.33個月。T細胞反應可以預測腫瘤生物標志物和ctDNA清除率的降低,并且它們與復發或死亡風險降低(86%)密切相關。?
此外,在兩個最高劑量隊列中(包括接受推薦的2期劑量(10mg)的患者),T細胞應答率為100%。對于高于中位T細胞應答水平的患者,中位無復發生存期尚未達到,而T細胞應答水平低于中位水平的患者為4.01個月,這在統計學上是一個顯著進步。?

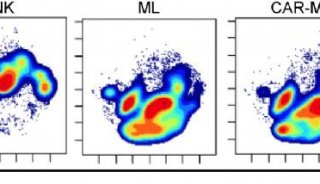
在大多數患者中,ELI-002 2P誘導了強大的mKRAS特異性T細胞反應?
更重要的是,沒有患者在治療后出現劑量限制性毒性、細胞因子釋放綜合征或任何治療后出現的3級以上不良事件。其中,在試驗中最常見的不良事件是疲勞(24%),注射部位反應(16%)和肌肉疼痛(12%)。重要的是,ELI-002 2P是一種現貨型癌癥疫苗,這意味著它不需要根據個人進行專門配制,具有生產成本低和可用性高的優點。?

ELI-002 2P治療后參與者的不良事件總結?
總的來說,這項1期臨床試驗展示了癌癥疫苗ELI-002 2P的療效、免疫原性安全性和推薦2期劑量,并證明ELI-002 2P可以有效緩解結直腸癌和胰腺癌患者的腫瘤復發,增加患者生存率。?
基于這些令人鼓舞的1期臨床試驗結果,研究團隊將于今年晚些時候開展2期臨床期試驗,進一步測試針對其他KRAS突變的ELI-002 2P腫瘤疫苗新配方。?
(來源:生物世界)?
原文出處:Pant S, Wainberg ZA, Weekes CD, Furqan M, Kasi PM, Devoe CE, Leal AD, Chung V, Basturk O, VanWyk H, Tavares AM, Seenappa LM, Perry JR, Kheoh T, McNeil LK, Welkowsky E, DeMuth PC, Haqq CM, O'Reilly EM. Lymph-node-targeted, mKRAS-specific amphiphile vaccine in pancreatic and colorectal cancer: the phase 1 AMPLIFY-201 trial. Nat Med. 2024 Feb;30(2):531-542. doi: 10.1038/s41591-023-02760-3. Epub 2024 Jan 9. PMID: 38195752; PMCID: PMC10878978.?
? 鏈接:https://pubmed.ncbi.nlm.nih.gov/38195752/?