銀屑病新藥!療效擊敗安進Otezla!
deucravacitinib是一種新型、口服、選擇性TYK2抑制劑,具有一種獨特的作用機制。

斑塊型銀屑病
百時美施貴寶(BMS)近日宣布,美國食品和藥物管理局(FDA)和歐洲藥品管理局(EMA)已分別受理了抗炎藥TYK2抑制劑deucravacitinib的新藥申請(NDA)和營銷授權申請(MAA):用于治療中度至重度斑塊型銀屑病(PsO)成人患者。FDA已將NDA的《處方藥用戶收費法(PDUFA)》目標日期定位2022年9月10日。此外,日本厚生勞動省(MHLW)也已受理了deucravacitinib用于成人治療中度至重度斑塊型銀屑病、膿皰型銀屑病、紅皮病型銀屑病的NDA。
deucravacitinib是一種首創(first-in-class)、口服、選擇性酪氨酸激酶2(TYK2)抑制劑,具有一種抑制IL-12、IL-23、1型干擾素途徑的獨特作用機制,該藥是處于臨床研究評估治療多種免疫介導性疾病的第一個TYK2抑制劑。

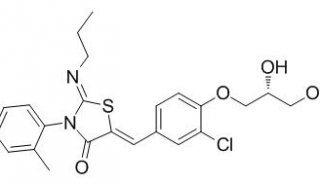
deucravacitinib化學結構式
deucravacitinib的監管申請,基于2項關鍵3期臨床試驗(POETYK PSO-1,POETYK PSO-2)的陽性結果。這2項試驗在中度至重度斑塊型銀屑病成人患者中開展,將deucravacitinib(6mg,每日口服一次)與安慰劑和Otezla(apremilast,30mg,每日2次)進行了對比。
結果顯示,2項試驗均達到了共同主要終點和次要終點:deucravacitinib與安慰劑、Otezla相比在皮損清除、癥狀負擔、生活質量方面表現出顯著的具有臨床意義的改善,包括在第16周與安慰劑和Otezla相比有顯著更高比例的患者達到銀屑病面積和嚴重程度指數相對基線改善至少75%(PASI75)、靜態醫師整體評估(sPGA)評分為皮損完全清除或幾乎完全清除(sPGA 0/1)、在第24周與Otezla相比有更高比例的患者達到PASI75和sPGA 0/1并維持至第52周。該研究中,deucravacitinib安全性和耐受性良好,不良事件導致的停藥率低,沒有臨床意義的實驗室異常。。
百時美施貴寶免疫和纖維化開發高級副總裁Jonathan Sadeh表示:“對于中重度斑塊狀銀屑病患者來說,迫切需要更有效、耐受性更好的口服療法,因為許多患者仍然沒有得到充分治療,甚至沒有得到治療。2項關鍵3期POETYK-PSO試驗的結果表明,deucravacitinib有潛力提高適合系統治療的患者群體的口服護理標準。我們期待著繼續與FDA和EMA合作,盡快將deucravacitinib帶給患者和醫生。”
-
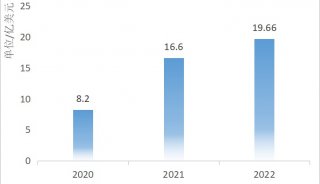
市場商機

-
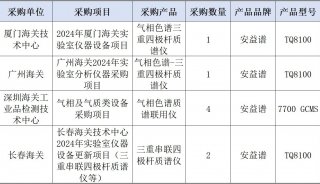
企業風采
-
焦點事件
-
項目成果